卢修斯万塞维/缬更昔洛韦(Valganciclovir)中文说明书详细!
万塞维/缬更昔洛韦
适应症
1、成人患者:
①艾滋病患者CMV视网膜炎的治疗;
②预防高危肾脏、心脏和肾胰腺移植患者的巨细胞病毒疾病。
2、儿科患者:
高危肾脏和心脏移植患者CMV疾病的预防。
用法用量
标准剂量 :盐酸缬更昔洛韦片口服给药,应与食物同服(参见药代动力学特点-吸收)。盐酸缬更昔洛韦片可迅速大量的转化成更昔洛韦。以更昔洛韦测定的盐酸缬更昔洛韦片的生物利用度比更昔洛韦胶囊高10倍,因此应严格遵守以下所述的盐酸缬更昔洛韦片用量和用法说明(参见注意事项和药物过量)。
CMV视网膜炎的诱导治疗 :对于活动性CMV视网膜炎患者,推荐剂量是900 mg(两片450 mg的片剂),每天2次,服21天。延长诱导治疗可能增加骨髓毒性的危险性(参见注意事项)。
CMV视网膜炎的维持治疗 :在诱导治疗后,或对于非活动性CMV视网膜炎患者,推荐剂量是900 mg(两片450 mg的片剂),每天1次。视网膜炎恶化的患者可重复诱导治疗(参见诱导治疗)。
移植患者CMV感染的预防 :已接受实体器官移植的患者,推荐剂量是900 mg(两片450 mg的片剂),每天1次,从移植后10天内开始,直至移植后100天。
特殊剂量指南肾功能不全病人 :应密切检测血清肌酐或肌酐清除率水平。应根据肌酐清除率按照以下所示(参见特殊人群的药代动力学和注意事项)进行剂量调整。CrCl≥ (greater than or equal to) 60 mL/min者,诱导剂量为900 mg,每天2次 ;维持剂量为900 mg,每天1次。CrCl为40-59 mL/min者,诱导剂量为450 mg,每天2次 ;维持剂量为450 mg,每天1次。CrCl为25-39 mL/min者,诱导剂量为900 mg,每天1次 ;维持剂量为900 mg,隔天1次。CrCl为10-24 mL/min者,诱导剂量为900 mg,隔天1次 ;维持剂量为900 mg,每周2次。
按下面公式可根据血清肌酐估算肌酐清除率 :男性=[140-年龄(岁) x 体重(公斤)÷(72) x [0.011 x 血清肌酐(umol/L)]。女性=0.85 × 男性数值。
进行血液透析的病人 :对于进行血液透析的病人(CrCl<10 mL/min),无法给出推荐剂量,因此盐酸缬更昔洛韦片不能用于此类患者(参见特殊人群的药代动力学和注意事项)。严重白细胞减少,中性粒细胞减少,贫血,血小板减少和全血细胞减少的病人 :盐酸缬更昔洛韦片(或更昔洛韦)治疗的病人有发生严重白细胞减少、中性粒细胞减少、贫血、血小板减少、全血细胞减少、骨髓抑制和再生障碍性贫血的病例。如果中性粒细胞绝对计数少于500个/uL,血小板计数少于25,000个/uL,或血红蛋白少于 8 g/dl,都不能开始盐酸缬更昔洛韦片的治疗(参见警告,注意事项和不良反应)。
特殊人群用药
1、妊娠期
口服给药后,缬更昔洛韦(前药)转化为更昔洛韦(活性药物),因此,预计VALCYTE具有与更昔洛韦相似的生殖毒性作用。在动物研究中,更昔洛韦对怀孕小鼠和家兔造成母胎毒性和胚胎-胎儿死亡率,对家兔的致畸性是人类暴露量的两倍。尚无关于孕妇使用VALCYTE或更昔洛韦以确定是否存在药物相关风险的可用人体数据。这些人群发生重大出生缺陷和流产的背景风险尚不清楚。
体内外人体胎盘模型的数据显示,更昔洛韦可穿过人体胎盘。这种转移是通过被动扩散进行的,在1至10毫克/毫升的浓度范围内没有饱和转移。
2、哺乳期
目前尚无有关缬更昔洛韦(前药)或更昔洛韦(活性药物)在人乳中的存在、对母乳喂养婴儿的影响或对乳汁分泌的影响的数据。动物实验数据表明,更昔洛韦会从哺乳期大鼠的乳汁中排出。美国疾病控制和预防中心建议感染艾滋病毒的母亲不要用母乳喂养婴儿,以避免产后传播艾滋病毒的风险。建议哺乳期母亲在使用 VALCYTE 治疗期间不建议进行母乳喂养,因为哺乳期婴儿可能会出现严重不良事件,而且可能会传播 HIV。
3、具有生殖潜力的男性和女性
具有生育能力的女性在开始使用VALCYTE前应接受妊娠检测。
避孕:
1)女性
由于VALCYTE具有诱变和致畸潜能,因此应建议具有生育能力的女性在治疗期间和使用VALCYTE治疗后至少30天内采取有效的避孕措施。
2)男性
由于VALCYTE具有诱变潜力,建议男性在使用VALCYTE治疗期间和治疗后至少90天内使用避孕套。
不孕症:
VALCYTE 的推荐剂量可能会导致暂时性或永久性的女性和男性不孕症。
4、儿童使用
VALCYTE口服溶液和片剂适用于预防4个月至16岁的小儿肾移植患者和1个月至16岁有患CMV疾病风险的小儿心脏移植患者的CMV疾病。
在4个月至16岁的儿科肾移植患者中使用VALCYTE口服溶液和片剂预防CMV疾病是基于两项针对4个月至16岁患者的单臂、开放标签、非比较性研究。研究1是对小儿实体器官移植患者(肾脏、肝脏、心脏和肾脏/胰脏)进行的安全性和药代动力学研究。VALCYTE在移植后10天内每日给药一次,移植后最长给药100天。研究2是一项安全性和耐受性研究,在小儿肾移植患者中,VALCYTE在移植后10天内每天给药一次,最长时间为移植后200天。这些研究的结果得到了先前在成人患者中进行的疗效展示的支持。
将VALCYTE口服溶液和片剂用于预防1个月至16岁小儿心脏移植患者的CMV疾病是基于两项研究(上述研究1和研究3),并得到了先前在成人患者中的疗效证明 。研究3是一项 VALCYTE 的药代动力学和安全性研究,研究对象是年龄小于 4 个月的小儿心脏移植患者,这些患者连续两天各接受一次 VALCYTE 口服液。根据现有的儿科和成人患者的药代动力学数据,我们建立了一个基于生理学的药代动力学(PBPK)模型,以支持年龄小于 1 个月的心脏移植患者的用药。然而,由于新生儿模型预测的不确定性,VALCYTE 不适用于该年龄组的预防。
VALCYTE口服溶液和片剂在儿童中预防 CMV 疾病的安全性和有效性尚未得到确定,包括小儿肝移植患者、小于 4 个月的肾移植患者、小于 1 个月的心脏移植患者、患有 CMV 视网膜炎的小儿艾滋病患者以及患有先天性 CMV 感染的婴儿。
5、老年用药
尚未对 65 岁以上的成人进行 VALCYTE 口服液或片剂的研究。VALCYTE 的临床研究未包括足够数量的 65 岁及以上受试者,因此无法确定他们的反应是否与年轻受试者不同。一般而言,老年患者的剂量选择应谨慎,通常应从剂量范围的低端开始,这反映了肝功能、肾功能或心功能下降以及伴随疾病或其他药物治疗的频率较高。众所周知,VALCYTE 会通过肾脏大量排泄,因此肾功能受损的患者发生毒性反应的风险可能更高。由于肾脏清除率随年龄增长而降低,因此在给药 VALCYTE 时应考虑患者的肾脏状况。应监测肾功能并相应调整剂量。
6、肾功能损害
肾功能损害患者接受VALCYTE给药时,建议减少剂量。
对于接受血液透析(CrCl 低于10毫升/分钟)的成人患者,不应使用 VALCYTE 片剂。成人血液透析患者应按照剂量减少算法使用更昔洛韦。
7、肝功能损害
尚未对肝功能受损患者服用 VALCYTE 的安全性和有效性进行研究。
注意事项
以更昔洛韦测定的盐酸缬更昔洛韦片的绝对生物利用度比更昔洛韦胶囊高10倍。盐酸缬更昔洛韦片不能1:1的代替更昔洛韦胶囊。
以前应用更昔洛韦胶囊要改用盐酸缬更昔洛韦片片剂的病人,应被告知:如果服用超过处方剂量的盐酸缬更昔洛韦片,有药物过量的危险。(参见用量用法,药物过量)。在治疗过程中建议监测全血细胞计数和血小板计数。有严重白细胞减少,中性粒细胞减少,贫血和/或血小板减少的病人,建议采用血细胞生长因子治疗和/或考虑暂停服药(参见特殊剂量指南和不良反应)。对肾功能不全的病人,需要按照肌酐清除率调整剂量(参见特殊剂量指南和特殊人群的药代动力学)。
对已进行血液透析的病人(CrCl;10mL/min),无法给出推荐剂量。因此盐酸缬更昔洛韦片不能用于此类患者(参见特殊剂量指南和特殊人群的药代动力学)。应用盐酸缬更昔洛韦片和/或更昔洛韦后有报道出现惊厥、镇静、头晕、共济失调和/或精神错乱。如果这些情况发生,可能会影响需要精力集中的活动,包括病人驾驶汽车和操作机器的能力。
在合用亚胺培南-西司他丁(泰能)和更昔洛韦的病人中有发生惊厥的报道。盐酸缬更昔洛韦片不应该与泰能合用,除非可能获得的益处高于潜在的危险性(参见药物相互作用)。
齐多夫定(Zidovudine)和盐酸缬更昔洛韦片单独应用都可能引起中性粒细胞减少和贫血。有些病人可能不能耐受全量合用这两种药(参见药物相互作用)。
在与盐酸缬更昔洛韦片合用时,去羟肌苷(Didanosine)的血浆浓度可能会升高;因此应密切监测病人的去羟肌苷毒性(参见药物相互作用)。合用盐酸缬更昔洛韦片和其他已知有骨髓抑制或与肾功能不全有关的药物时,会导致毒性增加(参见药物相互作用)。
药物相互作用
尚未使用缬更昔洛韦进行体内药物相互作用研究。然而,由于缬更昔洛韦会迅速且广泛地转化为更昔洛韦,预计缬更昔洛韦会出现与更昔洛韦相关的药物间相互作用。在肾功能正常的患者中进行了更昔洛韦的药物间相互作用研究。VALCYTE和其他经肾脏排泄的药物联合给药后,肾功能受损患者可能会出现更昔洛韦和联合给药药物浓度升高的情况。因此,应密切监测这些患者更昔洛韦和联合用药的毒性。
下表列出了更昔洛韦与已确定的和其他潜在的显著药物相互作用。
表:更昔洛韦已确定的和其他潜在的显著药物相互作用
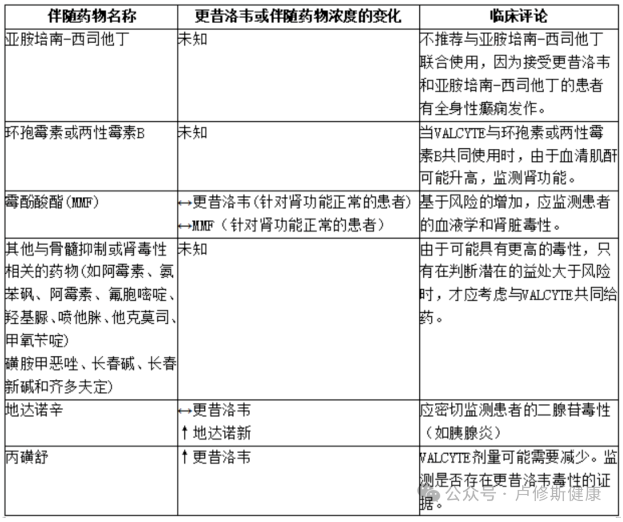
药物过量
使用 VALCYTE 片剂的经验:
过量服用 VALCYTE 可能会导致肾毒性增加。由于更昔洛韦可透析,透析可能有助于降低过量服用 VALCYTE 患者的血清浓度。应保持足够的水分。应考虑使用造血生长因子。
从临床试验和上市后经验中收到了关于过量使用缬更昔洛韦后出现不良反应的报告,其中一些不良反应导致死亡。大多数患者都出现了以下一种或多种不良反应:
血液毒性:骨髓抑制,包括全血细胞减少、骨髓衰竭、白细胞减少、中性粒细胞减少、粒细胞减少
肝毒性:肝炎,肝功能异常
肾毒性:既往有肾功能损害、急性肾损伤、肌酐升高的患者血尿恶化
胃肠道毒性:腹痛、腹泻、呕吐
神经毒性:全身性震颤、癫痫
禁忌症
对缬更昔洛韦、更昔洛韦或制剂的任何组分有临床意义的超敏反应(如过敏反应)的患者禁用。
形状
片剂(Tablets)
贮存方法
贮存于20°C ~25°C (68°C ~77°F);允许范围为15~30°C (59–86°F)温度条件下短途运输。
