深入了解替尔泊肽的减重原理,地表最强的减肥药究竟好在哪?
替尔泊肽是一种GIP/GLP-1双靶点药物,作为一种单分子多肽,可选择性结合并激活GIP受体和GLP-1受体,这些受体为天然GIP和GLP-1的靶点。基于GIP序列改良的分子,它增加了GLP-1的活性,同时,其GIP活性大约是GLP-1的10倍。这种结合GLP-1和GIP的双靶点药物,通过两者的互补和协同作用,展现出显著的疗效。
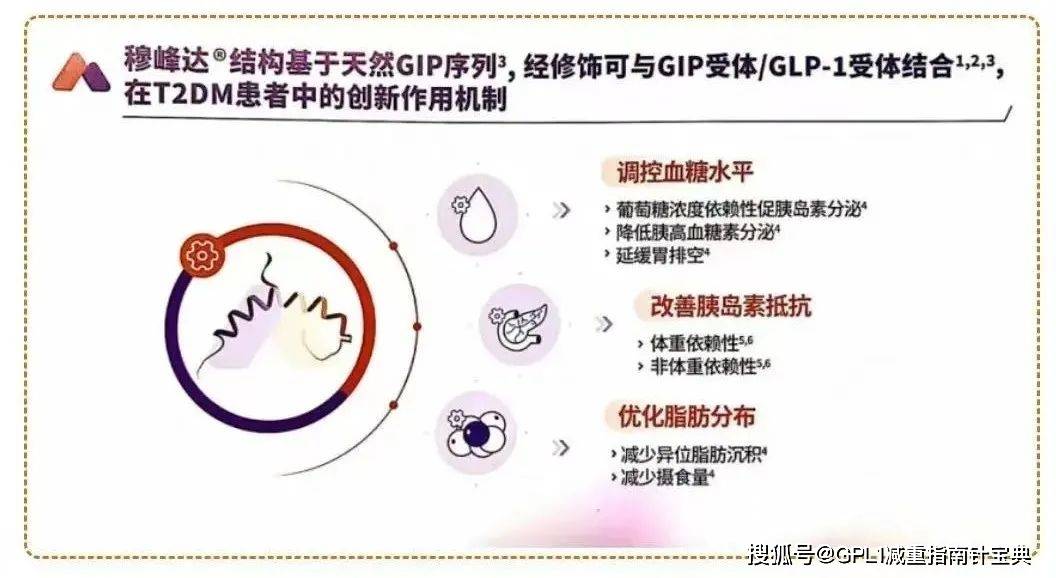
▍独特的双靶点作用机制
替尔泊肽是全球首个且目前唯一获批的葡萄糖依赖性促胰岛素多肽(GIP)/ 胰高糖素样肽 - 1(GLP - 1)受体激动剂,通过模拟两种激素,发挥双重作用。替尔泊肽在降糖、减重方面都超过了司美格鲁肽。
在降糖效果方面,多项临床研究显示替尔泊肽能显著降低2型糖尿病患者的HbA1c水平。替尔泊肽在SURPASS系列试验中,临床数据表现优异。在治疗2型糖尿病的患者方面,单药使用替尔泊肽后,患者糖化血红蛋白(HbA1c)平均降幅达2.0%-2.5%。
头对头比较研究表明,替尔泊肽在降低HbA1c方面可能略优于司美格鲁肽。SURPASS-2试验显示,替尔泊肽15mg剂量组较司美格鲁肽1mg剂量组在HbA1c降低方面有显著优势。该研究纳入约1800名2型糖尿病患者,结果显示替尔泊肽15mg组平均HbA1c降低2.46 %,而司美格鲁肽1mg组降低1.86%。此外,替尔泊肽在空腹血糖和餐后血糖控制方面也表现出更好的效果。
在减重效果方面,2024年12月5日,礼来公司公布了SURMOUNT-5临床3b期试验的头对头司美格鲁肽的主要结果。试验显示,接受Zepbound(替尔泊肽)治疗的受试者,平均减重50.3磅(22.8kg),而接受司美格鲁肽的受试者,平均减重33.1磅(15.0kg)。分析结果显示,替尔泊肽在减重效果上明显优于司美格鲁肽,减重幅度高出47%。具体来说,替尔泊肽组的受试者平均减重20.2%,而司美格鲁肽组为13.7%。此外,在72周的试验中,替尔泊肽组在主要终点和所有五项关键次要终点上均表现出显著优效性。在一个关键次要终点中,31.6%的替尔泊肽组受试者成功减重超过25%,而在司美格鲁肽中,只有16.1%的受试者达到了这一标准。
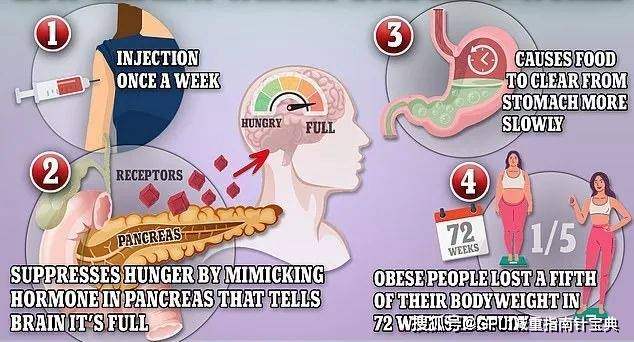
▍强力的食欲抑制功能
替尔泊肽通过作用于大脑中控制食欲的关键区域,优化神经信号的传递,使大脑更快接收到饱腹感信号。当进食时,该药物促使机体在摄入较少食物的情况下便产生满足感,从而自然减少食物摄取。这一机制并非依赖意志力来抑制食欲,而是通过生理层面的调节来重塑食欲感知,使个体更轻松地控制饮食量,降低热量摄入,从而实现体重管理。
当GLP-1和GIP激素与相应的受体结合时,它们会发挥生物学效应。GLP-1和GIP受体不仅在胰岛细胞中表达,也在中枢神经系统中有所分布。
替尔泊肽也通过激动GIP受体在减重方面显示了显著的效果。有研究表明,由人类或小鼠GIP序列改造而来的GIP类似物能够减少高脂饮食小鼠的食量,并导致体重下降。GIP受体激动剂能够阻止高脂饮食小鼠的体重增加,并且与利拉鲁肽联合使用时,能够实现更好的体重减轻效果。这些研究结果表明,GIP受体激动剂和GLP-1受体激动剂之间存在显著的协同作用。
临床前研究提示,GIP受体可在下丘脑中表达,参与中枢能量调节。在饮食诱导肥胖 (DIO) 小鼠的动物实验中,观察到外周注射GIP体重显著减轻,摄食量减少,且下丘脑进食中心弓状核和腹内侧核的cFOS表达 (神经元活性) 显著增加,提示GIP可能通过中枢神经系统的GIP受体降低体重和摄食量,帮助实现能量平衡。
▍延缓胃排空,增强饱腹感
GLP-1是一种由肠道L细胞在进食后分泌的激素。当替尔泊肽与GLP-1受体结合后,一系列生理调节机制随之启动。它精准地向大脑下丘脑区域传递信号,调节神经肽Y、POMC等神经递质的释放,增强饱腹感,从根源上减少食物摄取。此外,该药物还能有效延缓胃排空,使食物在胃内停留的时间延长,从而降低饥饿感的发生频率。临床研究数据显示,使用GLP-1受体激动剂的患者,其每日进食次数及每餐摄入量均有显著下降。
这种药物不仅通过作用于胃肠道延缓胃排空和胃肠蠕动,还能减少五肽胃泌素对胃酸分泌的刺激,从而进一步增强饱腹感并抑制食欲,减少食物摄入量。
另一方面,替尔泊肽对血糖调节也有积极作用。由于食物缓慢进入肠道,葡萄糖吸收更加平稳,避免了血糖骤升及随后的饥饿感,从而进一步降低进食频率与热量摄入。
▍促进能量消耗与代谢优化
替尔泊肽还能够在一定程度上提高基础代谢率,促进能量消耗,即使在静息状态下,机体也能燃烧更多热量,并促使脂肪更高效地分解供能,从而增强减重效果。
GIP和GLP-1在胰腺的作用也有所不同。GIP不仅能调节糖代谢,还能调节脂代谢,这对于控制血糖和血脂都非常重要。此外,GIP在皮下脂肪组织中的表达量很高,这意味着它在脂肪代谢中扮演着重要角色。GIP有助于促进体内脂肪的再平衡和再分布,提高脂肪组织的储存能力,同时减少异常脂肪堆积,这是含有GIP的双靶点药物相较于单靶点药物的一个显著优势。它促进内脏白色脂肪中解耦连蛋白 1(Ucp1)的表达,加快其向棕色脂肪转化,并促进棕色脂肪产热,进而不影响摄食而直接降低体重。
胰岛素抵抗指调节血糖水平的激素胰岛素的工作能力下降,易造成血糖失衡,引发2型糖尿病。替尔泊肽在2型糖尿病患者中对胰岛素敏感性和胰岛β细胞功能有影响。研究发现,替尔泊肽显著改善了胰岛β细胞功能和胰岛素敏感性。
▍临床数据佐证:减重效果可持续2年以上
临床研究数据充分证实了替尔泊肽卓越的减重效果。
替尔泊肽的SURMOUNT-1研究为期3年,数据显示,相较安慰剂,替尔泊肽(10mg和15mg)治疗肥胖或超重的糖尿病前期患者效果显著。72周时,使用安慰剂、5mg、10mg、15mg剂量组治疗,分别可以减重2.4%(2公斤)、16%(16公斤)、21.4%(22公斤)、22.5%(24公斤)。176周时,患者平均体重分别减少15.4%(5mg)、19.9%(10mg)和22.9%(15mg),安慰剂组仅减轻2.1%。停药17周后,患者体重开始回升,并出现2型糖尿病风险增加的趋势。然而,与安慰剂相比,替尔泊肽将糖尿病进展风险降低了88%。

2023年4月,SURMOUNT-2研究再次证明,较高剂量的替尔泊肽在72周内使2型糖尿病肥胖患者平均体重减少15.7%(15.6kg),较低剂量组减重13.4%(13.5kg)。其中,10mg和15mg组分别有81.6%和86.4%的患者减重超过5%,而安慰剂组仅为3.5%。
2023年11月,基于SURMOUNT-1和SURMOUNT-2的优异数据,FDA批准替尔泊肽用于肥胖治疗。
SURMOUNT-4试验显示,受试者在36周的替尔泊肽导入期内平均体重减轻21.1%,随后52周持续治疗期间再减轻6.7%,88周内总平均体重减轻26.0%。该试验专注于评估肥胖或超重的2型糖尿病患者在不同治疗阶段的减重效果。
2024年5月,替尔泊肽在中国超重或肥胖人群的III期研究SURMOUNT-CN结果公布,研究入组了210名中国患者。基线时受试者平均体重为91.8kg、平均BMI为32.3kg/m2、平均腰围为104.8cm。研究结果显示:第52周时10mg组、15mg组平均体重自基线分别降低13.6%、17.5%,均优效于安慰剂组(降低2.3%)。替尔泊肽10mg组、15mg组达到体重减轻≥5%的受试者比例分别为87.7%、85.8%,优效于安慰剂组(29.3%)。52周时替尔泊肽10mg组、15mg组平均腰围自基线分别减少11.4 cm、14.5cm,优效于安慰剂(减少2.6cm)。
替尔泊肽凭借其双重机制,更好地实现减重。快速减肥一直是这些GLP-1药物的标志,其作用在于让人们更早感到饱腹。在 GLP-1 问世之前,饮食和运动或减肥手术是减肥的主要途径,然而替尔泊肽的减重效果达到26.6%(29.2kg),它的出现已经改变了这一切。
*本文仅供医疗卫生专业人士参考
